Metody usuwania arsenu z wody

Technologie służące usuwaniu arsenu można podzielić na następujące grupy:
-
metody strąceniowe,
-
metody adsorpcyjne,
-
wymianę jonową i
-
procesy membranowe.
Niekiedy zachodzi konieczność stosowania kilku metod uzdatniania. Dzieje się tak szczególnie w przypadku, gdy arsen w wodzie występuje w dużych stężeniach. Sposób oczyszczania uwarunkowany jest również kwestiami ekonomicznymi [1]. Ze względu na różnorodność sposobów usuwania arsenu w poszczególnych w/w grupach, w niniejszym artykule omówione zostaną najbardziej powszechne metody, czyli metody strąceniowe. Zajmują one ważne miejsce wśród metod uzdatniania wody i polegają na usuwaniu niepożądanych domieszek w postaci trudno rozpuszczalnych osadów. Głównym celem tych procesów jest przekształcenie obecnych w wodzie rozpuszczalnych związków arsenu w połączenia nierozpuszczalne, a następnie usunięcie ich z oczyszczanej wody przez sedymentację i/lub filtrację. Zmniejszenie rozpuszczalności arsenu uzyskuje się poprzez przekształcenie chemiczne związków wyjściowych lub przez adsorpcję i wbudowanie się tych związków w powstające podczas procesu oczyszczania związki żelaza, glinu, manganu i wapnia [2].
Koagulacja/Filtracja
Podczas klasycznej koagulacji objętościowej połączonej z sedymentacją i filtracją, związki arsenu(III) usuwane są ze skutecznością od 20 do 90%, natomiast arsenu(V) od 60 do 100%.
Usuwanie arsenu metodą koagulacji prowadzi się przy użyciu soli żelaza lub glinu, takich jak: chlorek żelaza(III) FeCl3·6H2O, siarczan(VI) żelaza(III) Fe2(SO4)3·9H2O, siarczan(VI) glinu(III) Al2(SO4)3·18H2O, a także przy użyciu wapna CaO. Efekt procesu zależy od formy występowania arsenu w wodzie, rodzaju i dawki koagulantu, składu fizyczno - chemicznego wody, a przede wszystkim od wartości pH. Po dodaniu koagulantu do uzdatnianej wody powstają kłaczki wodorotlenków glinu i żelaza, na których adsorbowane są związki arsenu [1]. Podczas koagulacji solami glinu i żelaza na kłaczkach Al(OH)3 i Fe(OH)3 sorbowane są głównie trudno rozpuszczalne związki arsenu, stąd skuteczność ich usuwania jest największa w zakresie pH, przy którym rozpuszczalność Al(OH)3 i Fe(OH)3 jest najmniejsza i istnieje możliwość powstawania trudno rozpuszczalnych połączeń arsenu [3].
Przy jednakowych dawkach koagulantu i pH 5-7, efektywność usuwania arsenu z użyciem soli żelaza(III) jest znacznie wyższa niż w przypadku soli glinu. Poza tym w przypadku koagulantów glinowych duży wpływ ma odczyn wody. Powyżej pH=7 skuteczność soli glinu szybko maleje, podczas gdy sole żelaza mogą być stosowane do pH=8 [4]. Zależność tą przedstawiają poniższe rysunki 1 i 2.
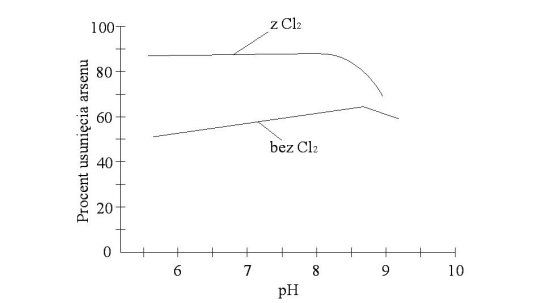
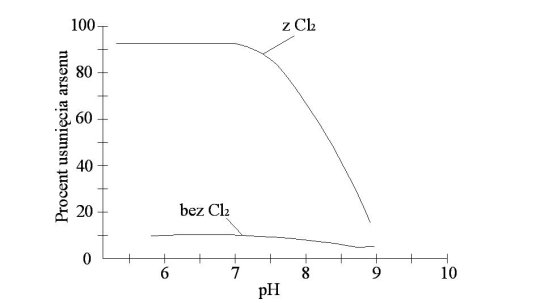
McNeil i Edwards odkryli, że rozpuszczalność i trwałość kłaczków odgrywa ważną rolę w usuwaniu arsenu. Po dodaniu koagulantu żelazowego, większość żelaza unosi się jako wodorotlenek żelaza. W przypadku koagulacji solami glinu, znaczna część dodanego glinu pozostaje w postaci rozpuszczonych kompleksów. Ponieważ tylko nierozpuszczalne wodorotlenki metali mogą pośredniczyć w redukcji arsenu, podczas procesów usuwania arsenu należy dokładnie rozpatrzyć rozpuszczalność glinu. Kompleksy glinu mogą przechodzić przez filtry i zmniejszać całkowity stopień usuwania arsenu z wody [6].
Generalnie trudniej usuwalne są związki As(III) niż As(V), dlatego przed procesem koagulacji zaleca się utlenienie arsenu(III) do arsenu(V) (uwzględnione na rysunkach 1 i 2). Powoduje to znaczne zwiększenie stopnia usuwania arsenu. Utlenianie może odbywać za pomocą chloru, jednak przy wyborze reagenta należy kierować się również możliwością powstawania produktów ubocznych.
Skuteczność usuwania związków arsenu w procesie koagulacji zależy również od obecności innych jonów w uzdatnianej wodzie. Mogą one współzawodniczyć z jonami arsenianowymi o miejsca aktywne na powierzchni wodorotlenków. Największy wpływ mają jony krzemianowe. Przy ich obecności, im wyższe pH tym niższa skuteczność usuwania arsenu z wody [2].
Utlenianie żelaza/manganu
Utlenianie żelaza i manganu jest procesem związanym z uzdatnianiem wód podziemnych o podwyższonej zawartości tych związków. Proces pod względem chemizmu jest identyczny z procesem koagulacji solami żelaza [1]. Następuje tu utlenienie Fe(II) do Fe(III) i Mn(II) do Mn(IV), w celu przekształcenia form rozpuszczalnych w nierozpuszczalne wodorotlenki tych metali. Reakcja zachodzi dzięki napowietrzaniu wody lub poprzez dodanie utleniacza (na przykład chloru). W trakcie odżelaziania i odmanganiania wody następuje usuwanie arsenu w wyniku współstrącania i adsorpcji na powstających nierozpuszczalnych związkach Fe(III) i Mn(IV).
Duże znaczenie przy redukcji arsenu ma żelazo. Podczas odżelaziania efektywność usunięcia arsenu jest rzędu 95%. Jeżeli mamy do czynienia z wodą zawierającą tylko związki żelaza, to skuteczność usuwania z niej arsenu jest znacznie wyższa niż z wody zawierającej tylko związki manganu. W wodach podziemnych stężenie manganu jest wielokrotnie niższe niż stężenie żelaza i najczęściej nie przekracza 0,5 mg/L [3]. Przeprowadzono badania, które wykazały, że odżelazianie/odmanganianie wody zawierającej powyżej 1,0mg Fe/L pozwala na zmniejszenie stężenia As(V) poniżej 5,0 μg/L [2].
Istotna redukcja arsenu odbywa się na złożu z piasku glaukonitowego (greensand). Materiałem aktywnym w „greensandzie" jest glaukonit, zielony, bogaty w żelazo minerał, który ma własności jonowymienne. Piasek glaukonitowy pracuje, dopóki jego ziarna nie pokryją się warstwą tlenku manganu, zwłaszcza ditlenkiem manganu(IV). Arsen usuwa się tu na zasadzie utleniania, wymiany jonowej i adsorpcji. Związki arsenu na zasadzie wymiany jonowej wymieniają się z tlenkiem manganu (przypuszczalnie OH- i H2O) znajdującym się na powierzchni ziaren. Utleniająca natura powierzchni manganowej zamienia As(III) na As(V), a następnie adsorbuje As(V). W rezultacie zredukowany Mn(II) jest uwalniany z powierzchni złoża. Efektywność tego procesu zależy od jakości wody uzdatnianej. Redukcja arsenu rośnie z 41% do ponad 80% jeżeli stosunek As/Fe rośnie z 0 do 20 [6].
Koagulacja wspomagana mikrofiltracją
Proces koagulacji wspomaganej mikrofiltracją (MF) nie wymaga fazy flokulacji. Do uzyskania wysokiej skuteczności wystarczy osiągnięcie w procesie szybkiego mieszania (do 20 s) kłaczków o średnicy 2-10 μm. Po dodaniu koagulantu (stosuje się głównie FeCl3) i mieszaniu woda kierowana jest na membranę filtracyjną o porach około 1 μm [7]. Zalety mikrofiltracji w porównaniu z konwencjonalną filtracją to:
-
bardziej efektywna bariera,
-
usunięcie mniejszych flokuł i
-
wzrost pojemności urządzeń [6].
Badania wykazały, że metoda ta pozwala na usunięcie arsenu w 95% przy stężeniu koagulantu 2,8 mg/L i przy pH 6-7. Poziom redukcji arsenu jest taki sam nawet przy bardzo dużym poziomie krzemionki w oczyszczanej wodzie.
Wysokoefektywna koagulacja
Przeprowadzone w latach 90' badania nad zastosowaniem wysokoefektywnej koagulacji uwzględniały wzrost dawki siarczanu glinu i chlorku żelaza z 10 do 30 mg/L i/lub spadek pH z 7,0 do 5,5. Okazuje się, że w procesie tym arsen(V) usuwany jest w ponad 90% (podczas zastosowania chlorku żelaza). Wysokoefektywna koagulacja jest bardziej skuteczna przy zastosowaniu soli żelaza w porównaniu z solami glinu. Koagulant glinowy może osiągnąć podobną skuteczność pod warunkiem redukcji pH wody [6].
Zmiękczanie wody wapnem
Twardość powodowana jest głównie przez związki wapnia i magnezu znajdujące się w wodzie. Dodanie wapna do wody powoduje wzrost pH, podczas którego wodorowęglan przekształca się w węglan i w rezultacie wapno wytrąca się jako węglan wapnia CaCO3. Gdy ilość węglanu wapnia jest niewystarczająca do usunięcia twardości do pożądanego poziomu, do wody dodaje się węglan sodu. Zmiękczanie polegające na usunięciu wapna zachodzi przy pH 9,0-9,5. W celu usunięcia magnezu, dodawany jest nadmiar wapna ponad poziom, przy którym wytrąca się ono jako węglan. Wodorotlenek magnezu Mg(OH)2 wytrąca się przy pH wyższym niż 10,5.
Podobnie jak przy koagulacji lepsze efekty otrzymuje się dla As(V). Badania wykazały, że przy pH10,5 As(V) usuwany jest prawie w 100%, a As(III) zaledwie w 20% (rysunek 3).
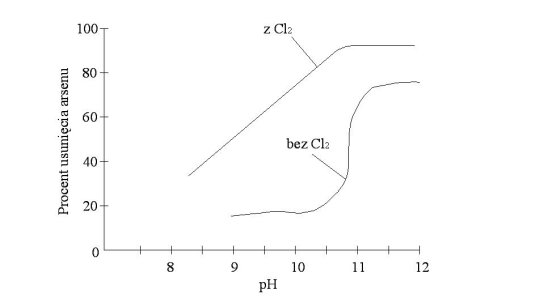
Lepsze efekty dla usuwania As(III) otrzymuje się przy pH11, ale nawet wtedy jego redukcja nie jest większa niż 75%. Wstępne chlorowanie wody zawierającej As(III), przed dodaniem wapna, pozwala na jego usunięcie w takim samym stopniu jak As(V) z wody niechlorowanej [1, 6].
Przeredagowała: Ewelina Puk
Literatura
[1] Piech, A.: „Występowanie i usuwanie związków arsenu z wód ujmowanych do celów pitnych", Praca doktorska, promotor: Granops, M., Politechnika Poznańska Wydział Budownictwa, Architektury i Inżynierii Środowiska, 2004
[2] Kociołek-Balaweider, E.; Ociński, D.: „Przegląd metod usuwania arsenu z wód", Przemysł Chemiczny, rok: 2006, T. 85, nr 1, s. 19 - 26
[3] Kowal, A.L.; Świderska-Bróż, M.: „Oczyszczanie wody", Wydanie 3, Warszawa, Wydawnictwo Naukowe PWN S.A., 1996
[4] Kowal, A.L.; Sozański, M.: „Podstawy doświadczalne systemów oczyszczania wód. Sedymentacja, koagulacja i filtracja", Wrocław, Wydawnictwo Politechniki Wrocławskiej, 1977
[5] Kartinen, E. O.; Martin, Jr.; Martin C. J.: „An overview of arsenic removal processes", Desalination, Volume: 103, Issue: 1 - 2, November, 1995, pp. 79 - 88
[6] United States Environmental Protection Agency, Office of Water: "Technologies and costs for removal of arsenic from drinking water", December 2000
[7] Chwirka, J. D.; Colvin, Ch.; Gomez, J. D.; Mueller, P. A., J. AWWA, Vol. 96, pp. 106, 2004